Автор: Денис Аветисян
Исследователи разработали систему SkinFlow, оптимизирующую визуальное представление данных для повышения точности и скорости дерматологической диагностики.
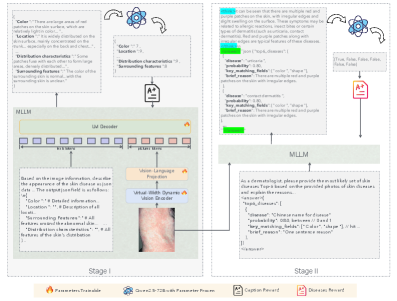
SkinFlow использует динамическое визуальное кодирование и двухэтапное обучение с подкреплением для эффективной передачи информации, достигая передовых результатов при меньшем размере модели.
Несмотря на впечатляющий масштаб современных больших визуально-языковых моделей, их эффективность в дерматологической диагностике часто снижается из-за неспособности выделить тонкие патологические признаки на фоне шума. В данной работе, представленной под названием ‘SkinFlow: Efficient Information Transmission for Open Dermatological Diagnosis via Dynamic Visual Encoding and Staged RL’, предлагается новый подход, рассматривающий диагностику как оптимизацию эффективности передачи визуальной информации. Разработанный фреймворк SkinFlow, сочетающий динамический визуальный энкодер и двухэтапное обучение с подкреплением, позволяет достичь передовых результатов на бенчмарке Fitzpatrick17k, превосходя значительно более крупные модели. Не является ли оптимизация потока информации и геометрической емкости более перспективным путем к точной медицинской диагностике, чем простое увеличение числа параметров?
Рассеянное Внимание: Преодолевая Поверхностный Взгляд
Несмотря на перспективность больших визуально-языковых моделей (LVLM) в дерматологической диагностике, часто наблюдается рассеянное внимание, препятствующее точной идентификации поражений. Данная особенность проявляется в неспособности моделей эффективно различать критически важные патологические сигналы от несущественной фоновой информации, что негативно сказывается на надежности постановки диагноза. Вместо фокусировки на ключевых признаках, LVLM склонны распределять внимание на всю область изображения, что приводит к снижению точности выявления тонких изменений, необходимых для своевременной диагностики и эффективного лечения кожных заболеваний. Таким образом, проблема рассеянного внимания становится существенным препятствием на пути к широкому внедрению LVLM в практическую дерматологию.
Ограничение возможностей больших визуально-языковых моделей в дерматологической диагностике объясняется их неспособностью эффективно отделять критически важные патологические сигналы от постороннего шума. В результате, модели склонны к ошибочной интерпретации изображений, поскольку не могут сфокусироваться на незначительных, но клинически значимых визуальных признаках, которые опытный врач сразу же замечает. Такая неспособность различать существенное от несущественного напрямую влияет на надежность диагностики, приводя к потенциальным ошибкам и задержкам в начале необходимого лечения. По сути, модели «теряются» в избыточности визуальной информации, не выделяя ключевые маркеры заболевания.
Современные подходы к диагностике дерматологических заболеваний с использованием компьютерного зрения часто оказываются неспособны уловить тонкие визуальные признаки, на которые обращают внимание опытные врачи-дерматологи. Это связано с тем, что ключевые диагностические детали — едва заметные изменения цвета, текстуры или границ поражения — могут быть зашумлены общими особенностями кожи или артефактами изображения. В результате, даже самые передовые алгоритмы могут давать ошибочные результаты, приводя к неправильному диагнозу и, как следствие, к задержке необходимого лечения, что особенно критично при выявлении злокачественных новообразований кожи.
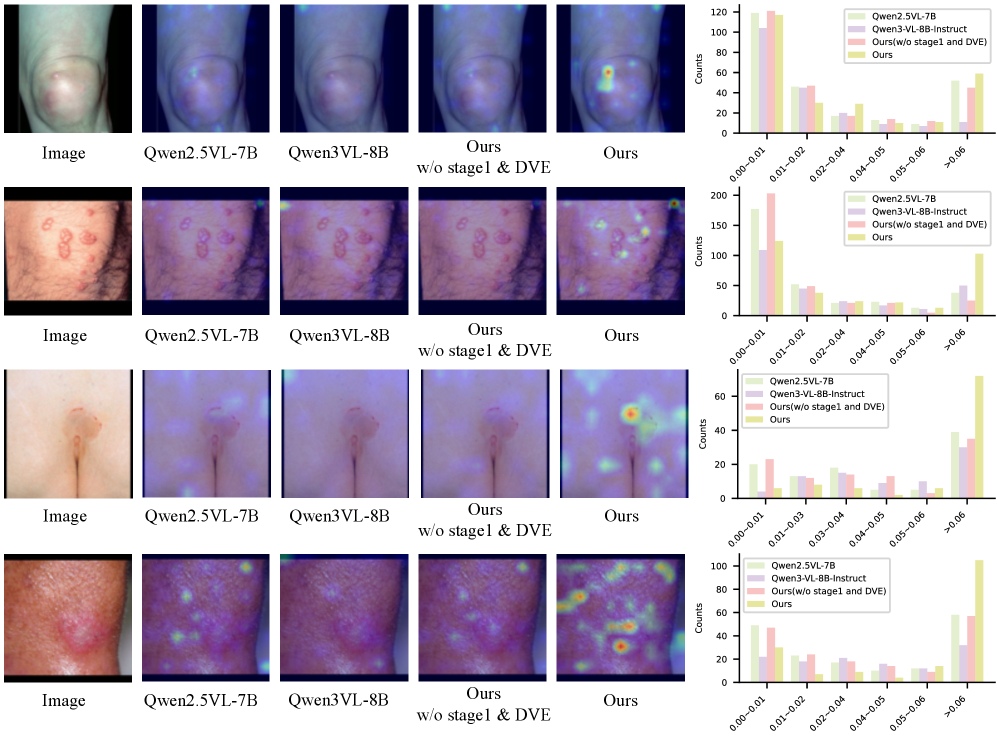
SkinFlow: Двухэтапная Оптимизация для Точной Диагностики
SkinFlow представляет собой новую двухэтапную систему обучения с подкреплением, разработанную для повышения точности дерматологической диагностики за счет максимизации передачи информации от изображения к конечному диагнозу. В основе подхода лежит идея оптимизации процесса преобразования визуальных данных в диагностические заключения, что достигается путем структурирования и акцентирования наиболее значимых признаков. Система ориентирована на повышение эффективности диагностики за счет более полного использования информации, содержащейся в медицинских изображениях, и минимизации потерь данных при преобразовании изображения в диагностический результат. Архитектура системы позволяет оптимизировать каждый этап процесса, от извлечения признаков до формирования диагноза, что обеспечивает более надежные и точные результаты.
Первый этап SkinFlow использует медицинское описание изображений для сжатия сложной визуальной информации в лингвистически интерпретируемые признаки. Этот процесс предполагает преобразование пиксельных данных в структурированное текстовое представление, описывающее ключевые визуальные элементы, такие как форма, текстура и цвет дерматологических образований. Полученные лингвистические признаки служат стандартизированным и компактным входом для второго этапа, обеспечивая более эффективную и целенаправленную обработку информации при постановке диагноза. Использование медицинского описания позволяет снизить вычислительную сложность и повысить интерпретируемость модели, поскольку обеспечивает представление изображения в виде понятных и структурированных данных.
Второй этап SkinFlow использует механизм диагностической доработки для реконструкции неявных патологических текстур в пространстве выходных данных, специфичном для конкретного диагноза. Этот процесс позволяет выделить и усилить критически важные признаки, которые могут быть недостаточно очевидны в исходном изображении. Реконструкция текстур осуществляется с учетом особенностей каждого диагноза, что позволяет более точно определить и визуализировать характерные изменения в коже. В результате достигается повышение четкости и информативности выходных данных, что способствует более надежной и точной диагностике.
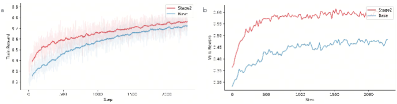
Динамическое Визуальное Кодирование: Усиление Сигнала для Диагностики
Динамическое визуальное кодирование (DVE) повышает отношение сигнал/шум визуальных признаков за счет адаптивного развертывания патологических многообразий. Этот процесс позволяет выявить тонкие диагностические сигналы, которые в противном случае могли бы быть скрыты в шуме. Развертывание многообразий происходит путем изменения представления данных, делая патологические случаи более различимыми и облегчая их идентификацию алгоритмами машинного обучения. Эффективно, DVE увеличивает контраст между здоровыми и патологическими состояниями в пространстве визуальных признаков, что приводит к повышению точности диагностики.
Виртуальное расширение размерности позволяет увеличить геометрическую ёмкость кодировщика изображений без увеличения числа его параметров. Данный подход реализуется посредством добавления дополнительных, виртуальных, измерений в пространство признаков, в котором кодировщик выполняет преобразования. Эти виртуальные измерения не требуют обучения отдельных весов, а формируются на основе существующих признаков, что позволяет расширить репрезентативную способность модели, не увеличивая вычислительную сложность или риск переобучения. Фактически, это позволяет кодировщику более эффективно отображать и различать сложные патологические структуры, улучшая точность диагностики.
Обучение данной системы осуществляется с использованием алгоритма Group Relative Policy Optimization (GRPO), представляющего собой эффективный метод обучения с подкреплением. GRPO позволяет ускорить процесс обучения и повысить производительность за счет оптимизации политики агента относительно групп состояний, что обеспечивает более стабильное и быстрое схождение алгоритма. В отличие от традиционных методов обучения с подкреплением, GRPO снижает дисперсию градиентов, что приводит к более эффективному использованию данных и сокращению времени, необходимого для достижения оптимальных результатов. Эффективность GRPO обусловлена его способностью к адаптации к сложным задачам и его масштабируемостью для обработки больших объемов данных.
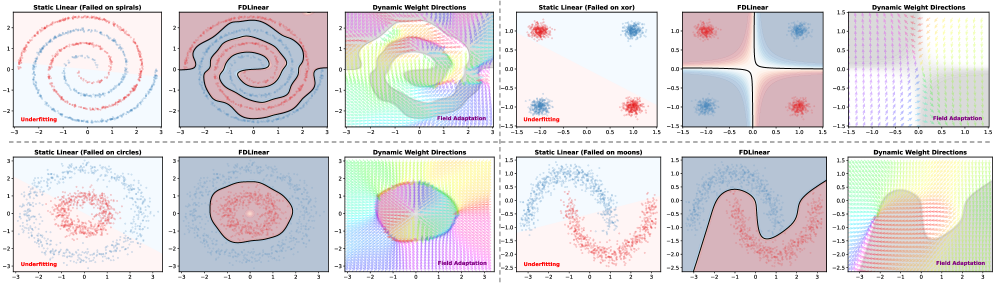
Клинически Обоснованная Валидация и Прирост Эффективности
Оценка SkinFlow проводилась с использованием Клинически Обоснованного Протокола, который уделял первостепенное внимание иерархии заболеваний и безопасности диагностики, применяясь к обширному набору данных Fitzpatrick17k. Такой подход позволил не просто измерить точность, но и убедиться в надежности системы при решении сложных диагностических задач. Приоритет иерархии заболеваний гарантировал, что система способна различать не только конкретные диагнозы, но и понимать их взаимосвязь, что критически важно для клинической практики. Использование Fitzpatrick17k, крупного и разнообразного набора данных, обеспечило всестороннюю оценку возможностей SkinFlow в различных дерматологических сценариях, подтверждая ее потенциал в качестве надежного инструмента поддержки принятия решений.
Результаты исследований демонстрируют значительное повышение точности Top-6, что свидетельствует об улучшенной способности разработанной системы к извлечению релевантной информации в сложных диагностических случаях. Повышенная точность Top-6 указывает на то, что система успешно определяет шесть наиболее вероятных диагнозов, причем правильный ответ входит в этот список в большем количестве случаев по сравнению с существующими моделями. Такой подход особенно важен при диагностике кожных заболеваний, где проявления могут быть разнообразными и неоднозначными, а точная идентификация заболевания требует учета множества факторов. Улучшенная способность к извлечению информации позволяет системе предлагать более полный и точный список дифференциальных диагнозов, что способствует повышению качества медицинской помощи и снижению вероятности диагностических ошибок.
В ходе оценки на эталонном наборе данных Fitzpatrick17k, система SkinFlow продемонстрировала значительное улучшение точности, достигнув прироста в 12.06% по показателю Top-1 и впечатляющего увеличения в 28.57% по показателю Top-6. Эти результаты свидетельствуют о повышенной способности системы к точному извлечению информации и дифференциальной диагностике в сложных клинических случаях. Превосходство SkinFlow над существующими передовыми моделями подтверждает ее потенциал в качестве надежного инструмента поддержки принятия решений для специалистов в области дерматологии и визуальной диагностики.
Исследования показали, что SkinFlow демонстрирует впечатляющую точность при диагностике кожных заболеваний, достигая показателя Top-1 в 29.19%. Этот результат значительно превосходит производительность передовых моделей, таких как GPT-5.2, опережая её на 10.95%, и Qwen3VL-235B, с отрывом в 12.06%. Такое существенное улучшение точности указывает на потенциал SkinFlow как надежного инструмента поддержки принятия решений в дерматологии, способного повысить эффективность и точность диагностики кожных заболеваний.
В ходе оценки, SkinFlow продемонстрировал значительное улучшение точности в задачах, требующих определения шести наиболее вероятных диагнозов — Top-6 accuracy составил 71.16%. Этот показатель на 28.57% превышает результаты, полученные с использованием модели Qwen3VL-235B, что свидетельствует о существенном прогрессе в эффективности системы. При тестировании на внутренней базе данных, точность SkinFlow достигла еще более высокого уровня — 79.21%, подтверждая стабильность и надежность фреймворка в различных клинических сценариях и подчеркивая его потенциал для повышения качества диагностики кожных заболеваний.
Исследование демонстрирует стремление к эффективной передаче информации, что не может не вызывать уважения. Авторы SkinFlow, словно алхимики, пытаются выжать максимум из минимального набора данных, используя динамическое визуальное кодирование и обучение с подкреплением. Как заметил однажды Джеффри Хинтон: «Чем сложнее модель, тем больше вероятность, что она просто запоминает данные, а не понимает их». SkinFlow же, напротив, стремится к обобщению, к созданию компактного, но эффективного инструмента для дерматологической диагностики. В эпоху API и пустых CSV это выглядит особенно смело и, признаться, немного волшебно.
Куда же всё это ведёт?
Представленный фреймворк SkinFlow, безусловно, демонстрирует элегантность в уговаривании данных о дерматологической диагностике. Однако, не стоит забывать, что любое «оптимальное» кодирование — это лишь компромисс между необходимостью и доступным бюджетом информации. Уменьшение размера модели — похвально, но эта экономия — не истина в последней инстанции, а лишь временное перемирие с хаосом вычислительных ресурсов. Остается открытым вопрос: насколько эффективно эта «динамическая визуальная кодировка» справится с теми случаями, где «шум» — это не ошибка, а именно правда, не желающая быть упрощенной?
Будущие исследования, вероятно, столкнутся с необходимостью не просто оптимизировать передачу информации, а научиться распознавать её отсутствие. Потому что иногда, самое ценное — это не то, что модель «видит», а то, чего она не видит, и умеет ли она признать свою некомпетентность. Ключевым вызовом станет создание моделей, способных не только ставить диагноз, но и понимать границы своей осведомленности — ведь среднее по больнице — это не всегда истина, а лишь попытка сгладить углы.
В конечном счете, SkinFlow — это еще один шаг в направлении создания «умных» систем диагностики. Но помните: любая модель — это заклинание, которое работает до первого столкновения с реальностью. И чем сложнее заклинание, тем больше вероятность, что оно даст сбой в самый неподходящий момент.
Оригинал статьи: https://arxiv.org/pdf/2601.09136.pdf
Связаться с автором: https://www.linkedin.com/in/avetisyan/
Смотрите также:
- Искусственный интеллект в разговоре: что обсуждают друг с другом AI?
- Согласие роя: когда разум распределён, а ошибки прощены.
- Очарование в огненном вихре: Динамика очарованных кварков в столкновениях тяжелых ионов
- Язык тела под присмотром ИИ: архитектура и гарантии
- Разбираемся с разреженными автокодировщиками: Действительно ли они учатся?
- Квантовый импульс для несбалансированных данных
- Умная экономия: Как сжать ИИ без потери качества
- Редактирование изображений по запросу: новый уровень точности
- Эволюция под контролем: эксперименты с обучением с подкреплением в генетическом программировании
- Безопасность генерации изображений: новый вектор управления
2026-01-15 07:24