Автор: Денис Аветисян
Представлен BioFVM-B — библиотека, значительно ускоряющая многомасштабное моделирование клеток и позволяющая симулировать целые микроокружения органов.
Разработан высокопроизводительный решатель диффузии для агентного моделирования, использующий параллельные вычисления и алгоритм трехдиагональной матрицы.
Масштабирование клеточных моделей до реалистичных размеров опухолей представляет собой серьезную вычислительную задачу. В данной работе, посвященной ‘A novel scalable high performance diffusion solver for multiscale cell simulations’, предложена масштабируемая HPC-реализация для моделирования молекулярной диффузии, основанная на эффективной реализации конечно-объемного метода (FVM). Разработанная библиотека BioFVM обеспечивает ускорение до 200 раз и снижение потребления памяти до 36% по сравнению с существующими решениями, открывая новые возможности для моделирования сложных биологических систем. Не приведет ли это к созданию цифровых двойников заболеваний, позволяющих прогнозировать их развитие и тестировать новые методы лечения?
Точное моделирование микроокружения: вычислительные границы
Точное моделирование сложного взаимодействия между клетками и их микроокружением имеет первостепенное значение для понимания фундаментальных биологических процессов. Клетки не функционируют изолированно; их поведение, рост и дифференцировка глубоко зависят от физико-химических свойств окружающей среды, включая концентрацию питательных веществ, градиенты сигнальных молекул и механические силы. Изучение этих взаимосвязей необходимо для раскрытия механизмов развития, прогрессирования заболеваний, таких как рак, и разработки эффективных терапевтических стратегий. Понимание того, как клетки реагируют на изменения в микроокружении, позволяет предсказывать их поведение и манипулировать им, открывая новые возможности в области тканевой инженерии и регенеративной медицины. Более того, точное моделирование позволяет исследовать явления, которые трудно или невозможно изучить экспериментально, предоставляя уникальные insights в сложность биологических систем.
Традиционные вычислительные методы сталкиваются со значительными трудностями при моделировании взаимодействия клеток и их микроокружения в больших масштабах. Это связано с экспоненциальным ростом вычислительной нагрузки по мере увеличения количества клеток и сложности моделируемых процессов. Например, для симуляции даже относительно небольшого образца ткани требуется огромный объем памяти и процессорного времени, что делает исследования, требующие анализа больших популяций клеток или длительных временных интервалов, практически невозможными. Ограничения в вычислительных ресурсах вынуждают ученых упрощать модели, жертвуя точностью и детализацией, что может приводить к неверным выводам и препятствовать полному пониманию биологических явлений. В результате, возможности изучения сложных биологических систем, таких как рост опухолей, заживление ран или иммунный ответ, существенно ограничены текущими вычислительными возможностями.
Процесс диффузии и распада, моделирующий транспорт и потребление питательных веществ клетками в микроокружении, представляет собой значительную вычислительную задачу. Этот процесс требует отслеживания концентрации веществ в пространстве и времени, учитывая как распространение по законам диффузии, так и скорость их потребления клетками. Эффективное моделирование требует решения сложных дифференциальных уравнений в частных производных, что связано с огромными затратами памяти и времени процессора, особенно при моделировании больших объемов ткани или клеточных популяций. \nabla \cdot (D \nabla c) = -R — это упрощенное представление уравнения, где D — коэффициент диффузии, c — концентрация, а R — скорость реакции потребления. Повышение точности и масштабируемости моделирования этого процесса является ключевым для продвижения исследований в области биологии и медицины.
PhysiCell и BioFVM: многомасштабное моделирование в физической реальности
Платформа PhysiCell представляет собой мощную среду для проведения многомасштабного моделирования клеток, основанного на физических принципах. Она позволяет интегрировать различные уровни детализации — от молекулярных взаимодействий внутри клеток до влияния микроокружения и межклеточных коммуникаций. PhysiCell обеспечивает инструменты для определения геометрии, создания и управления клетками, а также для задания физических параметров, определяющих их поведение. Платформа поддерживает различные типы симуляций, включая рост опухолей, иммунные реакции и процессы заживления тканей, и может использоваться для изучения сложных биологических явлений in silico. Гибкость платформы позволяет адаптировать модели к конкретным задачам и исследовать влияние различных факторов на клеточное поведение.
Библиотека BioFVM является ключевым компонентом платформы PhysiCell, предназначенным для моделирования диффузии и распада субстратов в микроокружении клеток. BioFVM реализует численные методы решения уравнения диффузии \frac{\partial c}{\partial t} = D \nabla^2 c - k c , где c — концентрация субстрата, D — коэффициент диффузии, а k — скорость распада. Это позволяет численно моделировать транспорт питательных веществ, метаболитов, факторов роста и других молекул, влияющих на поведение клеток, с учетом их потребления и деградации в пространстве и времени. Библиотека оптимизирована для эффективного вычисления на больших сетках, что необходимо для моделирования сложных клеточных сообществ и тканей.
Метод уровней детализации (LOD) в составе библиотеки BioFVM значительно снижает вычислительную нагрузку при моделировании диффузии веществ в клеточном микроокружении. Суть метода заключается в адаптивном уменьшении разрешения сетки в областях с низким градиентом концентрации, что позволяет сократить количество решаемых уравнений без существенной потери точности. В областях с высоким градиентом, где важна точность, разрешение сохраняется на высоком уровне. Это позволяет эффективно использовать вычислительные ресурсы, моделируя диффузию в больших объемах и на длительных временных интервалах, что особенно важно для имитации сложных биологических процессов. Эффективность метода LOD напрямую зависит от корректного выбора критериев адаптации разрешения и обеспечения плавного перехода между уровнями детализации.
BioFVM-X и BioFVM-B: масштабирование к беспрецедентным разрешениям
BioFVM-X представляет собой расширение функциональности BioFVM, обеспечивающее возможность проведения распределенных вычислений. Это позволяет моделировать системы значительно большего размера и сложности, преодолевая ограничения, связанные с вычислительными ресурсами одного узла. Распределенные вычисления в BioFVM-X достигаются за счет разделения вычислительной области на несколько частей, которые обрабатываются параллельно на различных вычислительных узлах, что существенно увеличивает производительность и позволяет моделировать более крупные и детализированные биологические системы.
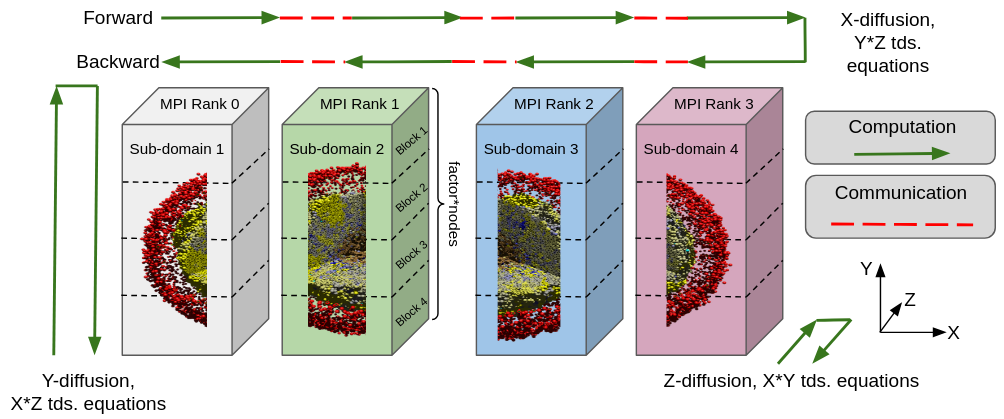
В BioFVM-X для реализации параллельных вычислений используется метод декомпозиции данных. Этот метод заключается в разделении вычислительной области на несколько поддоменов, каждый из которых обрабатывается отдельным процессором или вычислительным узлом. Разделение позволяет распределить нагрузку и выполнять вычисления одновременно, значительно сокращая общее время моделирования. Каждый поддомен содержит часть общей геометрии и связанных с ней данных, а обмен информацией между поддоменами осуществляется по мере необходимости для обеспечения корректности решения. Эффективность декомпозиции данных напрямую влияет на масштабируемость и производительность моделирования в BioFVM-X.
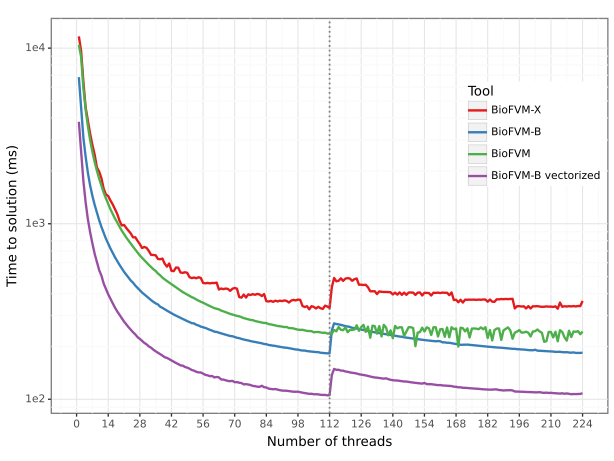
BioFVM-B представляет собой высокопроизводительное вычислительное решение, разработанное для дальнейшего увеличения масштабируемости моделирования. В его основе лежат параллельные модели программирования, такие как MPI (Message Passing Interface) и OpenMP. MPI обеспечивает распределенные вычисления на кластерах, позволяя использовать ресурсы нескольких вычислительных узлов, в то время как OpenMP используется для многопоточного программирования на отдельных узлах, что позволяет эффективно использовать многоядерные процессоры. Комбинация этих технологий позволяет BioFVM-B значительно превосходить BioFVM-X и BioFVM по скорости и масштабируемости при моделировании сложных биологических систем.
Для достижения прироста производительности в BioFVM-B активно используются SIMD (Single Instruction, Multiple Data) инструкции и векторизация. Данные методы позволяют выполнять одну и ту же операцию над несколькими элементами данных одновременно, значительно увеличивая пропускную способность вычислений. Векторизация включает в себя преобразование скалярного кода в векторный, что позволяет процессору эффективно использовать возможности параллельной обработки данных. Оптимизация кода с применением SIMD и векторизации позволяет добиться существенного ускорения выполнения сложных вычислительных задач, таких как моделирование биологических процессов, за счет более эффективного использования аппаратных ресурсов.
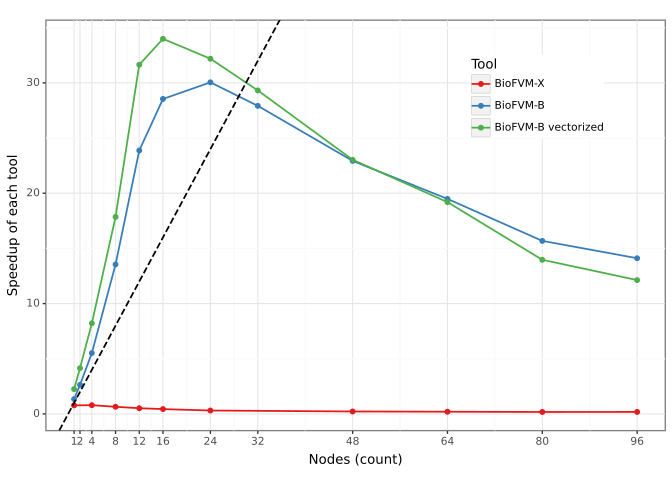
В ходе масштабного тестирования, BioFVM-B продемонстрировал значительное увеличение производительности по сравнению с предыдущими версиями. В наиболее сложном сценарии, моделирующем 21% печени, BioFVM-B обеспечил ускорение в 196.8 раза по сравнению с BioFVM-X и в 34.8 раза по сравнению с базовой версией BioFVM. Эти результаты подтверждают эффективность BioFVM-B как высокопроизводительного решения для моделирования сложных биологических систем, требующих значительных вычислительных ресурсов.
Проверка масштабируемости: слабая масштабируемость и за её пределами
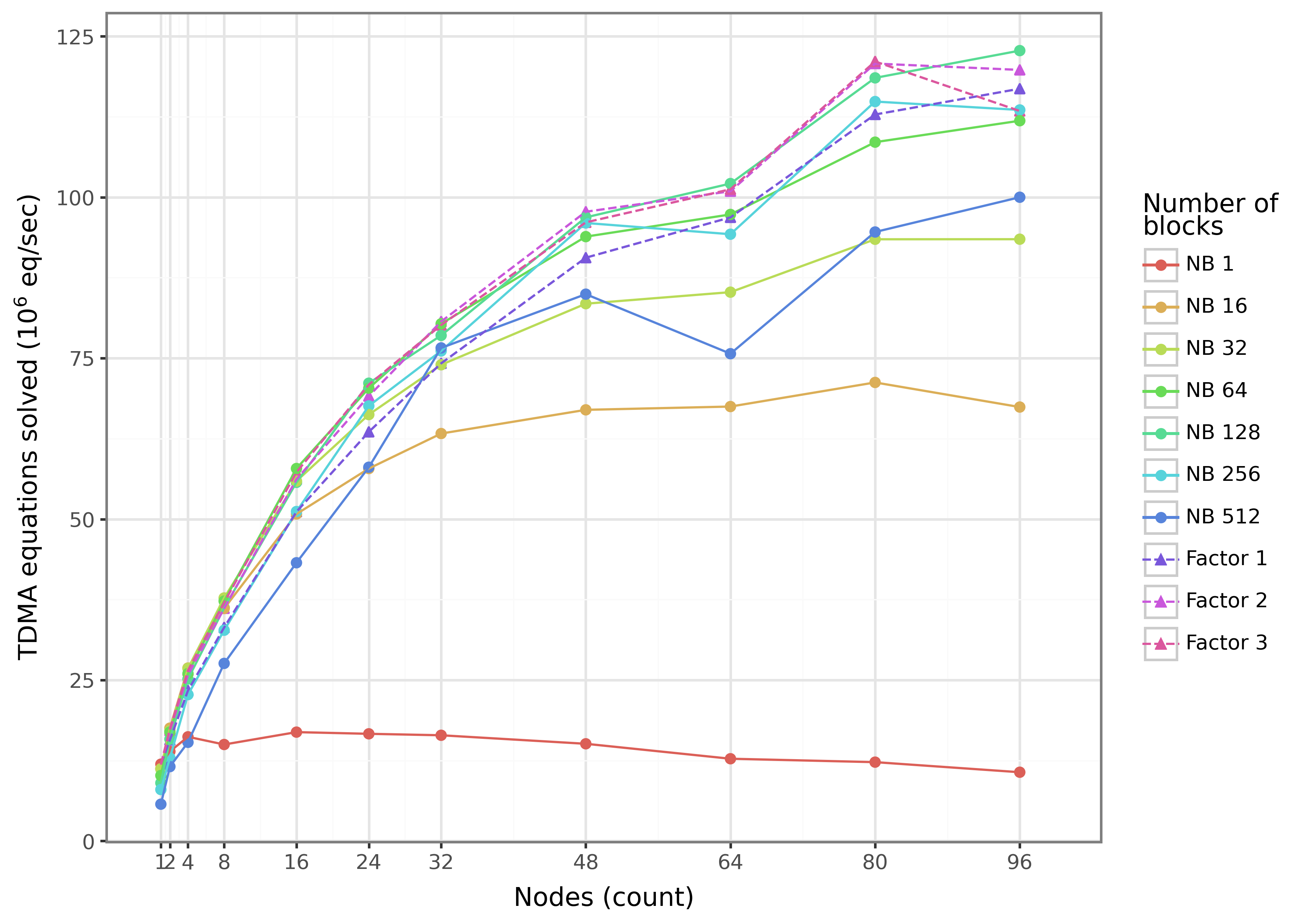
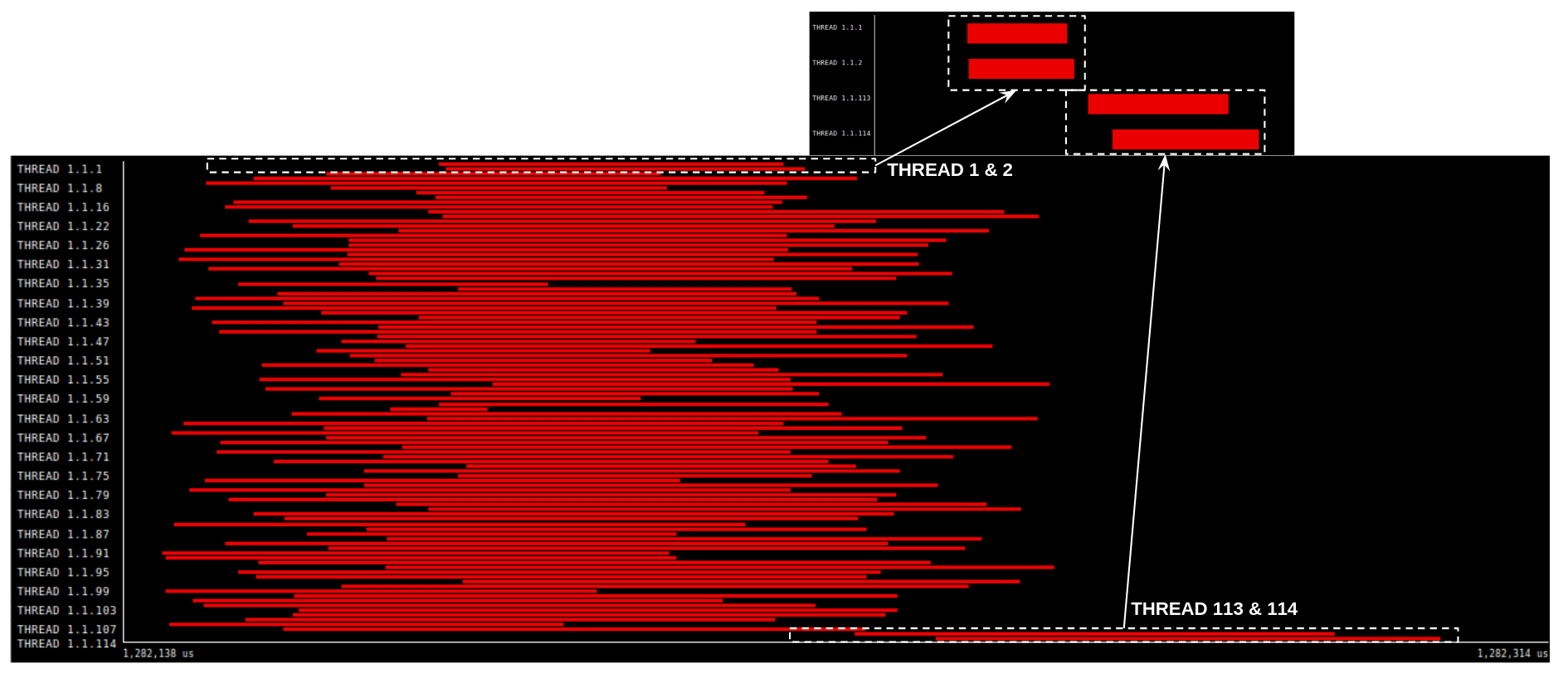
Оценка масштабируемости параллельных вычислений является ключевым аспектом при анализе эффективности BioFVM-B, и именно здесь на первый план выходит понятие «слабой масштабируемости». Данный показатель позволяет оценить, насколько производительность модели растет при одновременном увеличении как объема решаемой задачи, так и количества используемых процессорных ядер. В отличие от сильной масштабируемости, где размер задачи остается постоянным, слабая масштабируемость подразумевает пропорциональное увеличение задачи вместе с добавлением ресурсов. Таким образом, оценивается способность BioFVM-B поддерживать стабильную производительность при увеличении сложности модели и объемов данных, что критически важно для изучения биологических процессов на различных масштабах и с высокой детализацией. Положительные результаты в тестах на слабую масштабируемость подтверждают, что BioFVM-B эффективно использует доступные вычислительные ресурсы, обеспечивая возможность проведения масштабных симуляций.
Благодаря распределению вычислительной нагрузки, BioFVM-B предоставляет исследователям возможность изучать биологические вопросы в масштабах, ранее недоступных для моделирования. Это достигается за счет эффективной параллелизации вычислений, позволяющей обрабатывать значительно большие объемы данных и сложные системы. В результате, становится возможным моделировать биологические процессы, происходящие в больших тканях или организмах, исследовать взаимодействие между множеством клеток и молекул, а также анализировать влияние различных факторов на динамику биологических систем. Такой подход открывает новые перспективы для понимания сложных биологических явлений, например, прогрессирования раковых опухолей или процессов регенерации тканей, и способствует ускорению научных открытий в области биологии и медицины.
В основе моделирования начальных концентраций субстратов в BioFVM-B лежит использование гауссовского распределения. Этот подход позволяет реалистично отразить неоднородность распределения веществ в биологической среде, что существенно повышает точность симуляций. Вместо упрощенных, однородных предположений, программа учитывает вероятностную природу расположения молекул, имитируя естественные градиенты и флуктуации. Такой метод особенно важен при исследовании сложных биологических процессов, где локальные концентрации веществ играют критическую роль в определении клеточного поведения и реакций, например, при моделировании роста опухолей или формировании тканей.
В ходе сравнительного анализа было установлено, что BioFVM-B демонстрирует значительное снижение потребления оперативной памяти по сравнению с BioFVM-X. При моделировании с использованием одного субстрата, BioFVM-B потребовал на 40% меньше памяти, что особенно важно при работе с большими объемами данных. Даже при увеличении сложности модели и использовании 32 субстратов, BioFVM-B сохранил преимущество, обеспечив снижение потребления памяти на 15%. Данные улучшения позволяют проводить более масштабные и сложные симуляции, расширяя возможности исследования биологических процессов и требуя меньше вычислительных ресурсов.
Достижения в области оптимизации и масштабируемости BioFVM-B открывают принципиально новые возможности для изучения сложных биологических процессов и ускорения научных открытий в таких областях, как онкология и тканевая инженерия. Повышенная эффективность моделирования позволяет исследователям анализировать системы с беспрецедентным уровнем детализации, что особенно важно для понимания динамики роста опухолей, метастазирования и взаимодействия клеток в сложных тканевых структурах. Возможность моделировать более крупные и сложные биологические системы позволит получить новые данные о механизмах развития заболеваний, а также разработать более эффективные стратегии лечения и регенеративной медицины. Эти достижения, таким образом, способствуют прогрессу в фундаментальной биологии и практическом здравоохранении.
Данное исследование демонстрирует, что построение сложных систем, таких как моделирование клеточных микросред, требует не жесткого планирования, а скорее взращивания, подобно экосистеме. Авторы, оптимизируя структуры данных и используя параллельные вычисления в BioFVM-B, не просто создали инструмент, но и подготовили плодородную почву для будущих исследований в области мультимасштабного моделирования. Как отмечал Бертран Рассел: «Страх — это признак мудрости». В контексте разработки подобных систем, мониторинг и предвидение потенциальных сбоев — не признак неуверенности, а осознанный способ подготовки к неизбежным моментам истины, ведь настоящая устойчивость начинается там, где заканчивается иллюзия абсолютного контроля.
Что дальше?
Представленная работа, стремясь к ускорению многомасштабного моделирования клеток, неизбежно сталкивается с парадоксом: каждая оптимизация — это пророчество о будущей хрупкости. Масштабируемость — всего лишь слово, которым оправдывают усложнение. БиоFVM-B, как и любая архитектура, лишь откладывает момент, когда её границы станут очевидны. Вопрос не в скорости вычислений, а в способности системы адаптироваться к непредвиденному, к новым уровням детализации, к неожиданным взаимодействиям.
Истинная проблема заключается не в совершенствовании алгоритмов решения уравнений, а в понимании того, что идеальной архитектуры не существует. Это миф, необходимый, чтобы не сойти с ума, пытаясь предвидеть все возможные сценарии. Вместо погони за абсолютной производительностью, следует сосредоточиться на создании систем, способных к самоорганизации, к эволюции, к извлечению уроков из собственных ошибок.
Будущее многомасштабного моделирования лежит не в создании более быстрых решателей, а в разработке гибких, адаптивных экосистем, способных интегрировать разнородные данные и учитывать непредсказуемость биологических процессов. Все, что оптимизировано, однажды потеряет гибкость. Следует помнить, что системы — это не инструменты, а экосистемы. Их нельзя построить, только взрастить.
Оригинал статьи: https://arxiv.org/pdf/2602.05017.pdf
Связаться с автором: https://www.linkedin.com/in/avetisyan/
Смотрите также:
- Искусственный интеллект, который учится играть: новая платформа для стабильного обучения агентов
- Вероятностный компьютер на фотонных чипах: новая эра вычислений
- Наука из текста: извлечение знаний из научных публикаций
- Искусственный интеллект: хрупкость визуального мышления
- Ruyi2: Семейство языковых моделей для эффективного обучения и развертывания
- Сплетение света и времени: аттосекундная спектроскопия на квантовых парах
- Моделирование биомолекул: новый импульс от нейросетей
- Биомолекулярные связи: новый тест для искусственного интеллекта
- Самообучающиеся признаки: новый подход к машинному обучению
- Облачные вычисления для науки: гибкость и масштабируемость
2026-02-09 01:31