Автор: Денис Аветисян
Новая система на основе больших языковых моделей позволяет оценивать и улучшать способность ИИ предсказывать изменения в клетках под воздействием химических веществ.
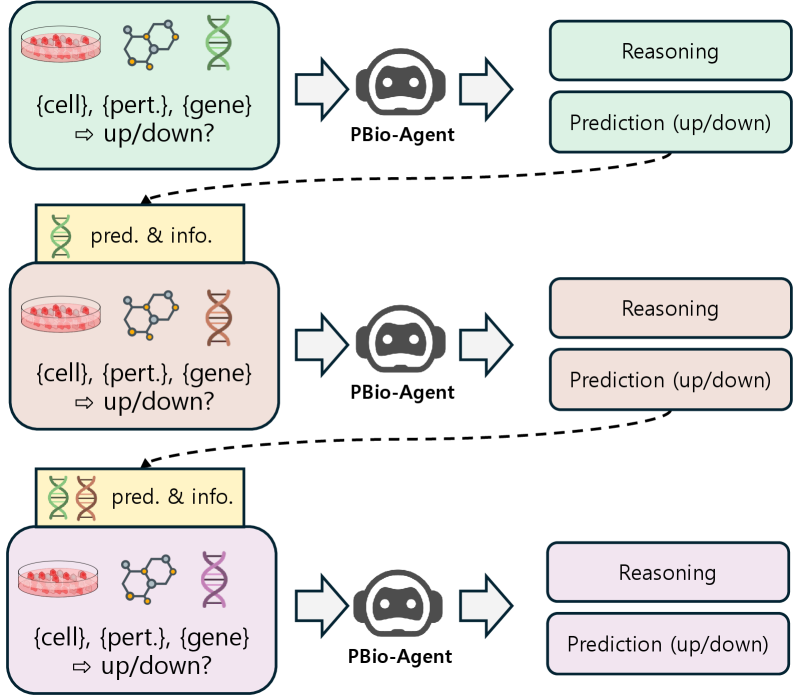
В статье представлена эталонная задача LincsQA и мультиагентная система PBio-Agent для оценки и улучшения возможностей больших языковых моделей в предсказании транскрипционной реакции клеток на химическое воздействие.
Предсказание ответа генов на биологические воздействия осложняется сложностью взаимосвязей и высокой размерностью данных. В данной работе, посвященной теме ‘Progressive Multi-Agent Reasoning for Biological Perturbation Prediction’, представлен новый бенчмарк LINCSQA для оценки способности моделей прогнозировать регуляцию генов при химических воздействиях в клеточных культурах. Ключевым результатом является разработанная система PBio-Agent, использующая многоагентный подход для последовательного анализа и уточнения знаний о биологических процессах. Способна ли эта архитектура значительно расширить возможности больших языковых моделей в сфере разработки лекарств и понимания сложных биологических систем?
Вызов механистического рассуждения в биологии
Прогнозирование изменений в экспрессии генов после воздействия на клетку является ключевой задачей современной биологии, однако существующие методы часто оказываются неспособными справиться со сложностью этой задачи. Биологические системы характеризуются огромным количеством взаимодействующих факторов, что делает точное предсказание последствий клеточных возмущений чрезвычайно трудным. Нередко, даже небольшое изменение в условиях может приводить к каскаду непредсказуемых эффектов, затрагивающих множество генов и метаболических путей. Существующие модели часто упрощают реальность, игнорируя тонкие нюансы регуляции и не учитывая сложные взаимосвязи между генами, белками и другими молекулами. В результате, предсказания, основанные на этих моделях, могут быть неточными или неполными, что затрудняет понимание фундаментальных биологических процессов и разработку эффективных терапевтических стратегий.
Существующие подходы к анализу биологических систем зачастую не способны адекватно отразить сложную взаимосвязь между различными факторами, что препятствует формированию точного механистического понимания происходящих процессов. Традиционные методы, как правило, рассматривают отдельные элементы и их непосредственное влияние, игнорируя косвенные эффекты, нелинейные взаимодействия и контекстную зависимость. Например, изменение экспрессии одного гена может инициировать каскад реакций, затрагивающих множество других генов и белков, при этом итоговый результат зависит от начального состояния клетки и влияния внешней среды. Неспособность учесть эти нюансы приводит к упрощенным моделям, которые плохо предсказывают поведение системы в новых условиях и затрудняют выявление истинных причинно-следственных связей. В результате, даже при наличии большого объема данных, понимание фундаментальных механизмов, управляющих жизнью, остается неполным.
Современная биология сталкивается с экспоненциальным ростом объемов данных, генерируемых высокопроизводительными технологиями. Это требует перехода от простых корреляционных анализов к сложным вычислительным стратегиям, способным выявлять причинно-следственные связи. Традиционные методы анализа часто оказываются неспособны справиться с огромным количеством параметров и взаимодействий, характерных для биологических систем. Разработка и применение алгоритмов машинного обучения, методов моделирования и системной биологии становятся необходимыми для интерпретации этих данных и построения адекватных моделей, позволяющих предсказывать поведение клеток и организмов в различных условиях. Такой подход открывает возможности для понимания фундаментальных биологических процессов и разработки новых методов лечения заболеваний.
PBio-Agent: Многоагентная система для прогнозирования
Система PBio-Agent использует многоагентный подход, в котором специализированные агенты совместно анализируют клеточные возмущения. Каждый агент предназначен для обработки конкретного аспекта данных или выполнения определенной задачи в процессе анализа. Взаимодействие между агентами осуществляется посредством обмена информацией и координации действий, что позволяет комплексно оценить влияние возмущений на клеточные процессы. Такая архитектура позволяет распределить вычислительную нагрузку и повысить эффективность анализа по сравнению с монолитными системами, а также обеспечивает модульность и расширяемость системы для интеграции новых типов данных и алгоритмов.
В основе системы PBio-Agent лежит интеграция структурированных биологических знаний, представленных в виде графа знаний (Knowledge Graph). Этот граф содержит информацию о генах, белках, метаболических путях, заболеваниях и их взаимосвязях, полученную из различных баз данных и научных публикаций. Агенты системы используют граф знаний для обоснования своих рассуждений и прогнозов, опираясь на установленные биологические связи и закономерности. Использование графа знаний позволяет агентам не только анализировать текущие данные о клеточных возмущениях, но и учитывать контекст, основанный на ранее установленных биологических фактах, что повышает точность и надежность прогнозов.
Последовательное рассуждение (Progressive Reasoning) в PBio-Agent предполагает построение прогнозов агентами поэтапно, с последовательным уточнением точности на каждом шаге. Вместо одномоментного предсказания, агенты формируют предварительные гипотезы, которые затем используются в качестве входных данных для последующих итераций рассуждений. Каждый агент, основываясь на предыдущих результатах и доступных знаниях, корректирует и улучшает прогноз, тем самым повышая общую надежность и точность предсказания биологических процессов и последствий клеточных возмущений. Этот итеративный процесс позволяет учитывать сложные взаимосвязи и динамику биологических систем, что приводит к более обоснованным и точным прогнозам.
В системе PBio-Agent каждый агент использует большую языковую модель (LLM) для обработки и интерпретации сложных биологических данных. LLM позволяет агентам понимать взаимосвязи между генами, белками и другими биологическими сущностями, представленными в графе знаний. Это обеспечивает возможность преобразования структурированных данных в осмысленные прогнозы о последствиях клеточных возмущений, предоставляя исследователям информацию, необходимую для принятия обоснованных решений и выявления потенциальных терапевтических стратегий. Использование LLM позволяет агентам не только анализировать данные, но и генерировать гипотезы и объяснения, тем самым расширяя возможности системы в области предсказательной биологии.
Валидация и производительность на эталонных наборах данных
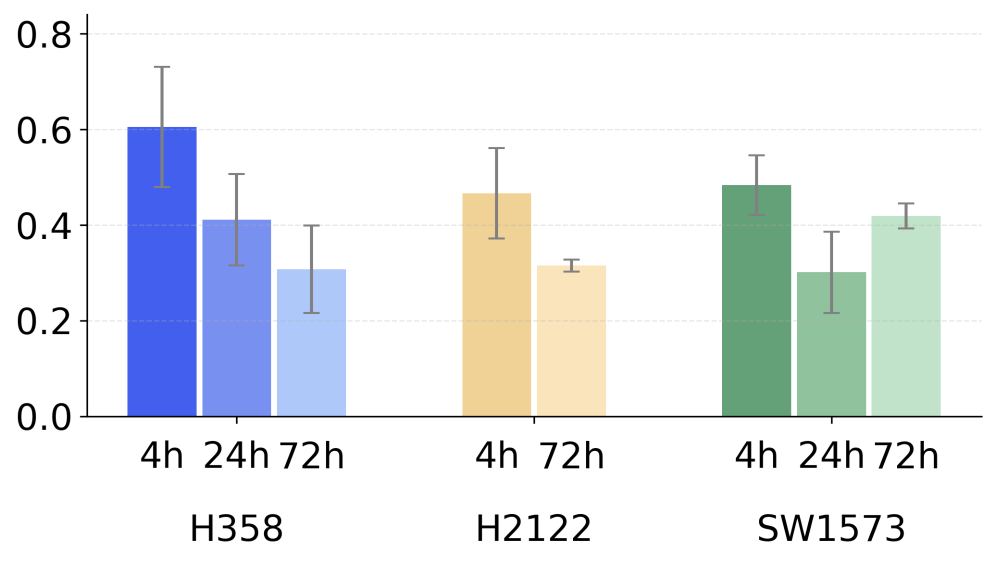
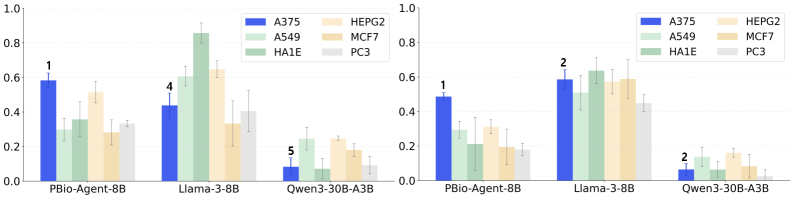
Фреймворк PBio-Agent был подвергнут тщательному тестированию на LincsQA, эталонном наборе данных для прогнозирования эффектов химических воздействий на оптовые клеточные культуры. Результаты демонстрируют передовые показатели в данной области. LincsQA предоставляет стандартизированную платформу для оценки моделей, предсказывающих изменения в экспрессии генов в ответ на химические соединения, и PBio-Agent показал свою эффективность в решении этой задачи, превосходя существующие методы в точности прогнозирования.
В ходе тестирования, фреймворк PBio-Agent продемонстрировал значение площади под ROC-кривой (AUROC) в 0.68 как для клеток HepG2, так и для клеток Jurkat. Данный показатель превосходит результаты, полученные с использованием существующих методов прогнозирования эффектов химических воздействий на клетки. Достижение AUROC в 0.68 подтверждает эффективность разработанного подхода в задаче предсказания реакций клеток на различные химические соединения и указывает на его превосходство над альтернативными решениями в данной области.
Внедрение метода Curriculum Learning позволило повысить эффективность обучения модели PBio-Agent за счет последовательного увеличения сложности используемых обучающих примеров. Этот подход предполагает начальное обучение на простых примерах, что облегчает освоение базовых закономерностей, и постепенный переход к более сложным случаям. Такая стратегия позволяет модели лучше обобщать данные и достигать более высоких показателей производительности, избегая перегрузки и обеспечивая стабильное обучение даже на сложных наборах данных. Использование Curriculum Learning в PBio-Agent способствовало улучшению результатов на бенчмарке LincsQA.
Расширение набора данных LincsQA позволило оценить способность PBio-Agent моделировать данные о возмущениях на уровне отдельных клеток. Изначально LincsQA был ориентирован на предсказания для совокупных клеток, однако модификация набора данных для включения данных о единичных клетках продемонстрировала более широкую применимость разработанной системы. Данный подход позволяет оценить способность модели учитывать гетерогенность клеточных популяций и предсказывать индивидуальные реакции на химические воздействия, что значительно расширяет возможности применения PBio-Agent в исследованиях, направленных на изучение клеточных механизмов и разработку персонализированных терапевтических стратегий.
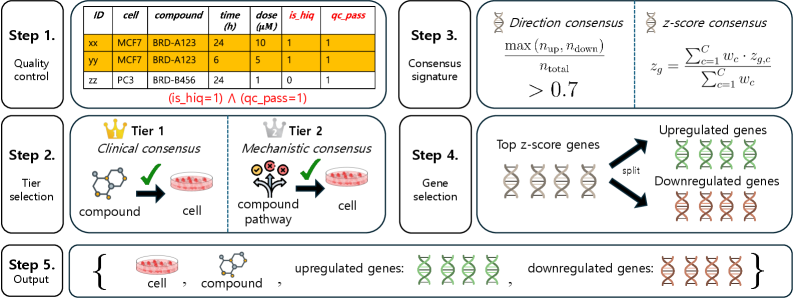
К пониманию механизма действия и разработке терапии
Возможность точного предсказания изменений в экспрессии генов, обеспечиваемая PBio-Agent, открывает новые перспективы в определении механизмов действия различных соединений. Данный подход позволяет исследователям не просто выявлять, как препарат влияет на клетку, но и понимать конкретные молекулярные пути, задействованные в этом процессе. Точность предсказаний, достигнутая благодаря интеграции данных о геноме и протеоме, существенно ускоряет процесс разработки лекарственных средств, позволяя целенаправленно оптимизировать их эффективность и минимизировать побочные эффекты. По сути, PBio-Agent выступает в роли мощного инструмента, способного дешифровать сложные биологические процессы и превращать теоретические знания в практические решения в области фармакологии и персонализированной медицины.
Исследование продемонстрировало высокую точность предсказаний системы PBio-Agent при анализе ингибиторов BRAF V600E. В ходе анализа препаратов дабрафениб и вемурафениб, система достигла относительного доминирования в 41.3% и 64.6% соответственно, что свидетельствует о ее способности учитывать специфические мутации в генах-мишенях. Такая чувствительность к мутационному статусу позволяет выявлять наиболее эффективные соединения и предсказывать их влияние на экспрессию генов, открывая возможности для разработки более целенаправленных и персонализированных методов лечения.
Исследования демонстрируют, что разработанная платформа способна учитывать клеточный контекст при анализе реакций на внешние воздействия. Это достигается за счет интеграции данных о специфике тканей, позволяя предсказывать различные ответы организма на одно и то же вещество в зависимости от его локализации. Например, препарат, эффективный в печени, может демонстрировать иные результаты в нервной ткани, и данная система способна это учитывать. Такой подход позволяет более точно идентифицировать мишени для терапии и разрабатывать персонализированные стратегии лечения, адаптированные к индивидуальным особенностям организма и конкретному типу ткани, что значительно повышает эффективность и безопасность фармакологических вмешательств.
Возможность точной идентификации мишеней и разработки персонализированных терапевтических стратегий представляет собой значительный прорыв в современной медицине. Благодаря комплексному анализу клеточного контекста и прогнозированию изменений в экспрессии генов, становится возможным учитывать индивидуальные особенности организма и специфику заболевания. Такой подход позволяет перейти от универсальных схем лечения к терапии, адаптированной под конкретного пациента, что значительно повышает ее эффективность и снижает риск побочных эффектов. В перспективе, это открывает путь к созданию лекарств, нацеленных на конкретные мутации и сигнальные пути, обеспечивая более целенаправленное и успешное лечение.
Исследование демонстрирует стремление к созданию систем, способных к комплексному анализу биологических процессов, что перекликается с идеей о том, что структура определяет поведение. В основе предложенного подхода — многоагентная система PBio-Agent, имитирующая взаимодействие различных компонентов клетки при химическом воздействии. Это позволяет моделировать сложные сценарии и прогнозировать реакцию клеток на лекарственные препараты, что является ключевым для открытия новых лекарств. Как однажды заметил Марвин Минский: «Наиболее ценные идеи часто оказываются самыми простыми». Простота и ясность в архитектуре системы PBio-Agent, где каждый агент представляет собой специализированный модуль, способствует более эффективному решению сложной задачи предсказания клеточных реакций.
Куда двигаться дальше?
Представленный подход, хотя и демонстрирует потенциал больших языковых моделей в предсказании клеточных ответов на химические воздействия, обнажает фундаментальную проблему: упрощение биологической сложности. Система, функционирующая как живой организм, не сводится к сумме ее частей, и попытки моделировать ее, полагаясь исключительно на текстовые данные, неизбежно наталкиваются на ограничения. Истинная предсказательная сила, вероятно, возникнет не из увеличения размера языковой модели, а из интеграции с другими модальностями данных — протеомикой, метаболомикой, и, что особенно важно, пространственной транскриптомикой.
Создание эталонного набора данных LincsQA — полезный шаг, но важно помнить, что сам эталон задает рамки. Необходимо расширять спектр рассматриваемых возмущений и клеточных типов, а также разрабатывать метрики, оценивающие не только точность предсказания, но и интерпретируемость полученных результатов. Устойчивость системы проявляется в ее способности адаптироваться, а не просто воспроизводить известные паттерны.
В конечном счете, будущее исследований лежит в понимании того, что модель — это лишь приближение к реальности. Элегантность решения не в его сложности, а в его способности выявить базовые принципы, определяющие поведение биологической системы. Иначе говоря, необходимо стремиться к ясности, а не к усложнению.
Оригинал статьи: https://arxiv.org/pdf/2602.07408.pdf
Связаться с автором: https://www.linkedin.com/in/avetisyan/
Смотрите также:
- Искусственный интеллект, который учится играть: новая платформа для стабильного обучения агентов
- Наука из текста: извлечение знаний из научных публикаций
- Моделирование биомолекул: новый импульс от нейросетей
- Вероятностный компьютер на фотонных чипах: новая эра вычислений
- Сплетение света и времени: аттосекундная спектроскопия на квантовых парах
- Биомолекулярные связи: новый тест для искусственного интеллекта
- Самообучающиеся признаки: новый подход к машинному обучению
- Искусственный интеллект: хрупкость визуального мышления
- Наука на Автопилоте: Система для Самостоятельных Исследований
- Робот-исследователь: новый подход к автономной навигации
2026-02-11 04:05