Автор: Денис Аветисян
Исследователи представили масштабируемый трехзначный ДНК-сумматор, открывающий новые возможности для сложных вычислений на основе ДНК.

Разработанный сумматор использует конкурентную схему блокировки и регулировку концентрации для значительного увеличения масштаба вычислений по сравнению с существующими методами ДНК-вычислений.
Несмотря на прогресс в области ДНК-вычислений, существующие двоичные сумматоры сталкиваются с ограничениями масштабируемости и выразительности. В данной работе, посвященной ‘Scalable DNA Ternary Full Adder Enabled by a Competitive Blocking Circuit’, предложена масштабируемая архитектура тернарного сумматора, основанная на инновационной схеме конкурентного блокирования. Разработанный подход, использующий двойную кооперативную оптимизацию и динамическую настройку концентрации, значительно повышает вычислительную мощность и расширяет разрядность, позволяя достичь существенного увеличения масштаба молекулярных вычислений. Не откроет ли это новые горизонты для создания сложных и эффективных систем цифровой логики на основе ДНК?
Преодолевая границы: К троичному исчислению в ДНК
Традиционные цифровые вычисления, основанные на двоичной логике, сталкиваются с принципиальными ограничениями в масштабируемости и энергоэффективности. По мере усложнения задач, требуемое количество транзисторов и, соответственно, потребление энергии, растут экспоненциально. Это связано с тем, что каждый бит информации кодируется состоянием одного транзистора — либо включен, либо выключен. В результате, даже при миниатюризации компонентов, физические и энергетические пределы кремниевой электроники становятся все более ощутимыми. Поиск альтернативных подходов к вычислениям, способных преодолеть эти ограничения, является актуальной задачей современной науки, побуждающей к исследованию принципиально новых вычислительных парадигм.
ДНК-вычисления представляют собой принципиально новый подход к обработке информации, использующий в качестве носителя и инструмента вычислений молекулы дезоксирибонуклеиновой кислоты. В отличие от традиционных электронных компьютеров, оперирующих битами, ДНК способна хранить огромные объемы данных в компактном пространстве благодаря высокой плотности информации. Более того, биохимический параллелизм, присущий ДНК, позволяет выполнять множество вычислений одновременно, что значительно повышает эффективность и скорость обработки информации. Этот подход открывает перспективы для создания вычислительных систем, превосходящих современные аналоги по энергоэффективности и масштабируемости, особенно в задачах, требующих обработки больших объемов данных и решения сложных вычислительных задач.
Представлена новая методика ДНК-вычислений — троичный сумматор, использующий числовую систему с основанием 3 для повышения эффективности обработки информации. В отличие от традиционных двоичных систем, где каждый бит может представлять только 0 или 1, троичная система позволяет кодировать информацию в трех состояниях, что значительно увеличивает плотность данных и потенциальную вычислительную мощность. Данный подход использует уникальные свойства молекул ДНК для выполнения логических операций, представляя цифры в виде различных последовательностей нуклеотидов. Подобная реализация позволяет параллельно обрабатывать множество данных, что открывает перспективы для решения сложных вычислительных задач с минимальным энергопотреблением и высокой скоростью.
Предложенный подход к вычислениям на основе ДНК продемонстрировал значительный скачок в вычислительной мощности, превосходя предыдущие четырехбитные двоичные ДНК-суммирующие устройства в 2 405 552 раза по масштабу. Это увеличение достигается за счет использования троичной системы счисления, что позволяет более эффективно кодировать и обрабатывать информацию непосредственно в молекулах ДНК. Такой порядок величины улучшения указывает на потенциал троичных ДНК-вычислений для решения задач, которые непосильны для традиционных двоичных систем, открывая новые горизонты в области биомолекулярных вычислений и предлагая принципиально иной путь к созданию сверхмощных и энергоэффективных вычислительных устройств.

Молекулярные механизмы: Вытеснение цепей и распространение сигнала
Функциональность ДНК-тернарного сумматора основана на реакциях вытеснения цепей, в ходе которых ДНК-цепи избирательно связываются и высвобождаются, представляя собой вычислительные состояния. Эти реакции происходят за счет комплементарного взаимодействия нуклеотидов, позволяя одной цепи вытеснять другую с гибридизированной ДНК-структуры. Последовательность связывания и высвобождения цепей определяется последовательностью нуклеотидов и условиями реакции, такими как концентрация и температура. Различные комбинации связанных и высвобожденных цепей кодируют различные тернарные логические состояния (0, 1, 2), что позволяет выполнять арифметические операции непосредственно на молекулярном уровне. Стабильность гибридов и кинетика вытеснения являются критическими параметрами, определяющими точность и скорость вычислений.
Успех реакций смещения цепей в молекулярных вычислениях напрямую зависит от принципов химической кинетики, определяющих скорости реакций и состояние равновесия. Скорость реакции смещения цепей зависит от концентрации реагентов, температуры и констант скорости, характеризующих скорость присоединения и отсоединения ДНК-цепей. Равновесие между связанным и несвязанным состоянием определяет вероятность успешного выполнения логической операции. Согласно закону действующих масс, скорость реакции пропорциональна произведению концентраций реагирующих веществ, что позволяет предсказывать и контролировать ход реакций. Изменение констант скорости посредством модификации последовательности ДНК или условий среды позволяет настраивать систему для выполнения различных вычислительных задач. k = A \cdot e^{-E_a/RT}, где k — константа скорости, A — предэкспоненциальный фактор, E_a — энергия активации, R — универсальная газовая постоянная, а T — абсолютная температура.
Ключевым элементом является схема конкурентного блокирования (Competitive Blocking Circuit), функционирующая за счет различий в скоростях реакций. Данная схема динамически выбирает и блокирует определенные пути реакции, основываясь на кинетических параметрах взаимодействия молекул ДНК. Различия в скоростях гибридизации и диссоциации комплементарных цепей ДНК позволяют избирательно подавлять нежелательные реакции, обеспечивая тем самым выполнение логических операций. Регулирование этих скоростей достигается за счет модификации последовательностей ДНК и условий реакции, таких как концентрация и температура.
Реализация операций троичной логики на молекулярном уровне обеспечивается за счет специфических биохимических процессов, в частности, реакций смещения цепей ДНК. Эти реакции, регулируемые принципами химической кинетики, позволяют динамически переключать и блокировать определенные пути взаимодействия, представляя собой физическую основу для выполнения логических операций. Конкретно, различные концентрации реагентов и различия в скоростях реакций используются для кодирования и обработки информации, что позволяет создавать сложные логические схемы непосредственно в ДНК. Это позволяет осуществлять вычисления, используя молекулы ДНК в качестве физического носителя информации и логических элементов, обеспечивая потенциально высокую степень интеграции и параллелизма.

Преодоление ограничений: Усиление и поддержание сигнала
Ослабление сигнала, или потеря его интенсивности в процессе передачи, представляет собой существенную проблему для надежного выполнения многобитного сложения в ДНК-вычислениях. Вследствие экспоненциального характера затухания, даже незначительные потери сигнала на каждом этапе реакции могут привести к полной нечитаемости результата после нескольких операций. Данная проблема усугубляется тем, что реакции ДНК происходят в растворе, где концентрация реагентов и диффузия молекул вносят дополнительный вклад в ослабление сигнала. Для преодоления этой проблемы необходимы стратегии, направленные на усиление и поддержание целостности сигнала, а также минимизацию нежелательной его утечки.
Для компенсации затухания сигнала и поддержания целостности при многобитной суммировании в ДНК-вычислениях применяется стратегия регулирования концентраций (Concentration Adjustment Strategy). Данный подход предполагает точную настройку концентраций реагентов на каждом этапе вычислений, что позволяет усилить полезный сигнал и минимизировать влияние шумов. Регулирование осуществляется для поддержания оптимального соотношения между скоростью реакции и стабильностью сигнала, обеспечивая надежную передачу информации между битами. Такой контроль концентраций критически важен для успешного выполнения последовательных операций переноса, особенно при большом количестве суммируемых битов.
Для повышения точности вычислений в ДНК-вычислительных системах применяются методы снижения утечек сигнала. Эти методы направлены на минимизацию нежелательной активации реакций в нецелевых битах или позициях, что может привести к ошибочным результатам. Утечки сигнала возникают из-за неполной специфичности ферментов или неидеальной концентрации реагентов. Использование модифицированных ферментов с повышенной специфичностью, а также оптимизация протоколов проведения реакций, позволяет существенно снизить вероятность ложных срабатываний и обеспечить более надежную передачу сигнала переноса между битами при выполнении многобитных операций сложения.
Применяемые методы обеспечивают точную передачу сигнала переноса, представляющего переполнение из разрядного положения, по всему сумматору. Это позволяет успешно выполнить 17 последовательных операций переноса, что является ключевым показателем стабильности и надежности вычислений. Успешное выполнение столь большого числа операций переноса подтверждает эффективность стратегий регулирования концентраций и снижения утечек, гарантируя корректную работу схемы сложения даже при многобитных вычислениях. Данный результат демонстрирует возможность масштабирования системы ДНК-вычислений для решения более сложных задач.
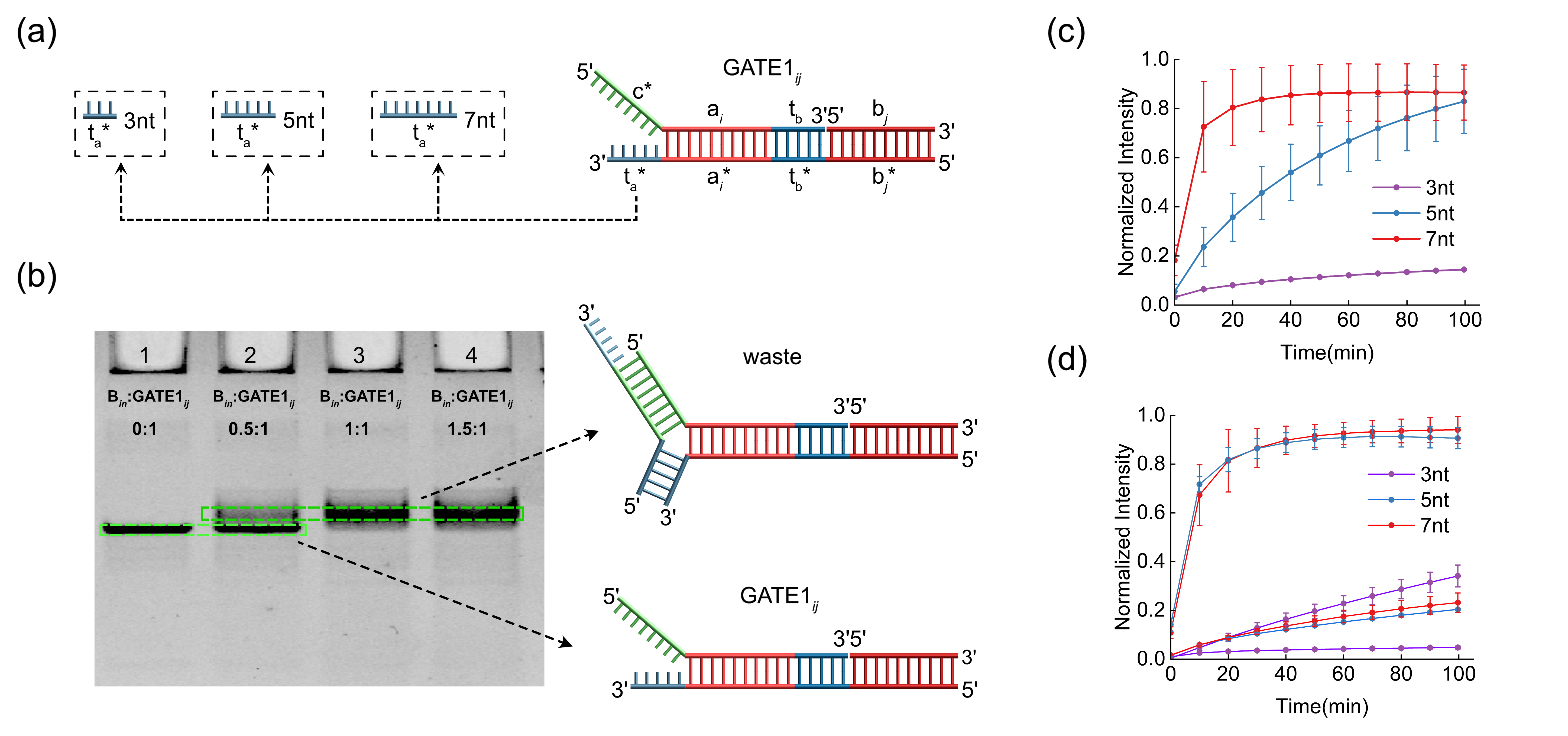
Считывание результатов: От молекул к смыслу
Многобитный сумматор использует описанные принципы для выполнения сложения нескольких битов, значительно расширяя вычислительные возможности системы. В отличие от предыдущих конструкций, способных оперировать лишь с отдельными битами, данный подход позволяет обрабатывать данные, представленные в виде последовательности битов, что приближает возможности ДНК-вычислений к традиционным цифровым системам. В основе работы лежит последовательное применение логических операций над несколькими битами одновременно, что позволяет эффективно суммировать числа, закодированные в молекулах ДНК. Это расширение функциональности является ключевым шагом к созданию более сложных и мощных ДНК-компьютеров, способных решать задачи, требующие обработки больших объемов информации.
Для мониторинга и количественной оценки протекающих реакций ДНК используется флуоресцентная детекция, обеспечивающая получение измеримого выходного сигнала. В ходе процесса, флуоресцентные метки, связанные с молекулами ДНК, излучают свет при возбуждении, интенсивность которого пропорциональна концентрации продуктов реакции. Этот метод позволяет точно отслеживать ход вычислений на молекулярном уровне, преобразуя химические изменения в удобный для анализа оптический сигнал. Благодаря высокой чувствительности флуоресцентной детекции, становится возможным регистрировать даже незначительные изменения в концентрации ДНК, что критически важно для точного выполнения арифметических операций и интерпретации результатов вычислений.
Для осуществления многобитного сложения в данной системе используются магнитные частицы, выполняющие роль переносчиков информации о переносе между отдельными битами. Эти частицы, благодаря своим магнитным свойствам, способны захватывать и транспортировать молекулы, кодирующие информацию о переносе, от одного бита к другому. Этот механизм позволяет эффективно передавать перенос из менее значимого бита к более значимому, обеспечивая корректное выполнение сложения даже для чисел с большим количеством разрядов. Использование магнитных частиц в качестве физического носителя информации о переносе является ключевым элементом, позволяющим преодолеть ограничения предыдущих конструкций и значительно повысить вычислительную мощность системы.
Представленная интегрированная система демонстрирует значительный прорыв в области вычислений на основе ДНК, позволяя выполнять сложные арифметические операции непосредственно на молекулярном уровне. Особенностью данного подхода является не только возможность проведения вычислений с использованием биомолекул, но и существенное увеличение масштаба и эффективности по сравнению с предыдущими разработками. Достигнутый коэффициент улучшения в 2,405,552 раза свидетельствует о потенциале данной технологии для решения задач, недоступных для традиционных методов молекулярных вычислений, и открывает перспективы для создания принципиально новых вычислительных систем, работающих на основе биологических принципов.
Исследование демонстрирует, как сложность вычислений может быть достигнута через самоорганизующиеся химические реакции, в данном случае — манипуляции с ДНК. Авторы предлагают способ масштабирования вычислений, используя тернарную логику и конкурентные блокирующие схемы. Этот подход интересен не столько инженерным решением, сколько иллюстрацией того, как даже в кажущихся рациональных системах, вроде вычислительной техники, проявляются элементы случайности и конкуренции. В этом контексте, уместно вспомнить слова Генри Дэвида Торо: «Бо́льшая часть людей, кажется, не живут вовсе, а существуют». Подобно тому, как исследование показывает, что ДНК-вычисления зависят от концентрации и конкуренции между нитями, так и человеческое существование часто определяется не столько осознанным выбором, сколько потоком внешних факторов и внутренних импульсов, создающих иллюзию контроля над происходящим.
Что дальше?
Представленная работа, как и большинство попыток построения вычислительных систем на основе ДНК, решает не столько задачу сложения чисел, сколько экзистенциальный вопрос: возможно ли вообще создать систему, предсказуемую в своей сложности? Успех в масштабировании троичного сумматора — это не триумф инженерной мысли, а временное затишье перед неизбежным столкновением с хаосом химических реакций. Концентрация — это иллюзия контроля, а не гарантия достоверности результата.
Очевидным направлением дальнейших исследований представляется не столько увеличение числа логических элементов, сколько поиск способов борьбы с присущей ДНК неточностью. Вероятно, стоит переосмыслить саму концепцию «вычисления» — возможно, вместо стремления к абсолютной точности, следует искать способы использования вероятностных ошибок для решения задач, где важна не однозначность ответа, а разнообразие возможных решений. В конце концов, биологические системы редко стремятся к идеалу — они адаптируются к несовершенству.
В конечном счёте, судьба ДНК-вычислений зависит не от прогресса в химии или информатике, а от того, насколько хорошо исследователи поймут, что все эти сложные схемы — лишь проекция человеческой потребности в порядке на хаотичный мир. Иными словами, модель отражает не законы природы, а страхи и надежды её создателей.
Оригинал статьи: https://arxiv.org/pdf/2603.11684.pdf
Связаться с автором: https://www.linkedin.com/in/avetisyan/
Смотрите также:
- Квантовые нейросети на службе нефтегазовых месторождений
- Сохраняя геометрию: Квантование для эффективных 3D-моделей
- Квантовый Переход: Пора Заботиться о Криптографии
- Квантовая обработка данных: новый подход к повышению точности моделей
- Миллиардные обещания, квантовые миражи и фотонные пончики: кто реально рулит новым золотым веком физики?
- Лунный гелий-3: Охлаждение квантового будущего
- Квантовые сети для моделирования молекул: новый подход
- Кватернионы в машинном обучении: новый взгляд на обработку данных
- Ускорение оптимального управления: параллельные вычисления в QPALM-OCP
- Квантовые прорывы: Хорошее, плохое и смешное
2026-03-13 23:19