Автор: Денис Аветисян
Исследование выявляет уникальные метаболические маркеры, позволяющие более точно диагностировать синдром дефицита внимания и гиперактивности.
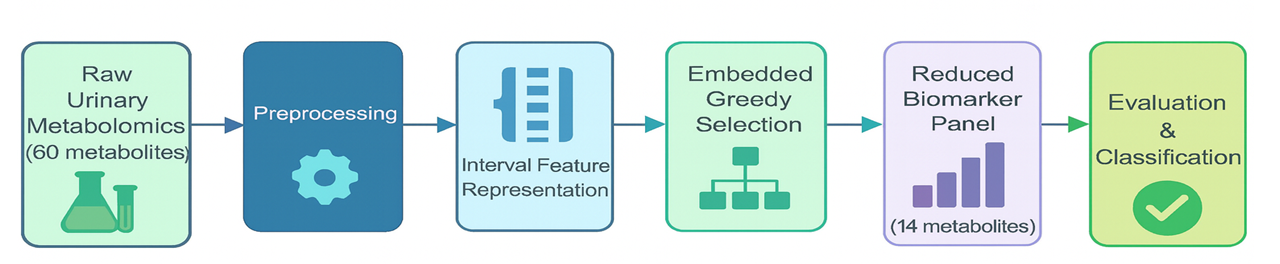
Применение интерпретируемых методов машинного обучения позволило выделить ключевые метаболиты в моче, различающие пациентов с СДВГ и контрольную группу.
Несмотря на широкую распространенность синдрома дефицита внимания и гиперактивности (СДВГ), объективные диагностические инструменты остаются ограниченными. В работе «Metabolomic Biomarker Discovery for ADHD Diagnosis Using Interpretable Machine Learning» представлен новый подход, интегрирующий анализ метаболома мочи с интерпретируемой системой машинного обучения для выявления биохимических маркеров, связанных с СДВГ. Разработанный классификатор на основе метода ближайшего соответствия (Closest Resemblance) продемонстрировал высокую точность (>0.97) и превзошел традиционные алгоритмы, выделив панель из 14 метаболитов, связанных с дофаминергической нейротрансмиссией и метаболизмом аминокислот. Сможет ли этот подход способствовать разработке точных и биологически обоснованных методов диагностики СДВГ в клинической практике?
Диагностика СДВГ: Между субъективностью и объективностью
В настоящее время диагностика синдрома дефицита внимания и гиперактивности (СДВГ) в значительной степени опирается на субъективные поведенческие оценки, основанные на критериях, представленных в DSM-5 и МКБ-11. Такой подход, несмотря на широкое распространение, сопряжен с риском неточностей, поскольку восприятие и интерпретация поведения могут варьироваться у разных специалистов. Субъективность оценок может приводить к ложноположительным или ложноотрицательным результатам, что, в свою очередь, задерживает начало необходимого лечения и поддержки для пациентов. Задержка в диагностике особенно опасна в детском возрасте, поскольку может негативно повлиять на академическую успеваемость, социальную адаптацию и общее развитие ребенка. В связи с этим, существует острая потребность в разработке более объективных и надежных методов диагностики СДВГ, которые бы минимизировали влияние субъективного фактора и позволяли своевременно оказывать помощь нуждающимся.
Традиционные методы диагностики, такие как нейровизуализация и электроэнцефалография, хоть и способны предоставить дополнительные сведения о функционировании мозга, сталкиваются с существенными ограничениями. Их высокая стоимость и ограниченная доступность делают их неприменимыми для широкого скрининга и ранней диагностики. Более того, наблюдаемые эффекты зачастую оказываются скромными, что затрудняет однозначную интерпретацию результатов и требует сопоставления с клиническими данными. Таким образом, несмотря на свою ценность в качестве вспомогательных инструментов, эти методы не обеспечивают надежной и объективной основы для выявления синдрома дефицита внимания и гиперактивности, подчеркивая необходимость поиска новых, более эффективных подходов к диагностике.
Существует острая необходимость в объективных и надежных биомаркерах, способных помочь в ранней и точной диагностике синдрома дефицита внимания и гиперактивности (СДВГ). В настоящее время диагностика в значительной степени полагается на субъективные оценки поведения, что может приводить к ошибкам и задержкам в начале лечения. Обнаружение биологических индикаторов, измеряемых объективными методами, такими как анализ крови или генетическое тестирование, позволит врачам более уверенно ставить диагноз, особенно у детей, где симптомы могут быть менее выраженными или трудноотличимыми от нормального поведения. Разработка таких биомаркеров не только повысит точность диагностики, но и откроет путь к персонализированным подходам к лечению, учитывающим индивидуальные особенности каждого пациента.
Понимание лежащих в основе синдрома дефицита внимания и гиперактивности (СДВГ) метаболических нарушений представляется ключевым фактором в обнаружении объективных биомаркеров, способных улучшить точность и своевременность диагностики. Исследования всё чаще указывают на то, что СДВГ связан с дисбалансом в метаболизме нейротрансмиттеров, энергетическом обмене и функционировании определенных метаболических путей. Однако выявление этих нарушений требует применения надежных аналитических методов, включающих высокочувствительные методы масс-спектрометрии, метаболомики и анализ данных с использованием передовых алгоритмов машинного обучения. Такой комплексный подход позволит идентифицировать специфические метаболические профили, характерные для СДВГ, и потенциально разработать новые диагностические инструменты, а также персонализированные стратегии лечения, учитывающие индивидуальные особенности метаболической регуляции у каждого пациента.
Метаболомный профиль: Путь к биомаркерам СДВГ
Метаболомика представляет собой всесторонний анализ малых молекул — метаболитов — в биологических образцах, позволяющий идентифицировать изменения в метаболических путях у лиц с синдромом дефицита внимания и гиперактивности (СДВГ). В отличие от геномики или протеомики, метаболомика предоставляет информацию о конечном продукте клеточных процессов и отражает текущее физиологическое состояние организма. Применение методов масс-спектрометрии и ядерного магнитного резонанса (ЯМР) позволяет одновременно детектировать и количественно оценивать сотни метаболитов, что даёт возможность выявить специфические метаболические профили, связанные с СДВГ. Идентифицированные изменения могут включать отклонения в концентрации нейротрансмиттеров, аминокислот и других важных биомолекул, указывая на дисрегуляцию метаболических процессов, характерную для данного расстройства.
Анализ метаболома мочи предоставляет неинвазивный метод оценки метаболических изменений, связанных с синдромом дефицита внимания и гиперактивности (СДВГ). В отличие от инвазивных процедур, таких как забор крови или спинномозговой жидкости, сбор мочи является простым и безболезненным для пациента, что значительно повышает применимость данного подхода в масштабных исследованиях. Неинвазивность делает возможным проведение многократных измерений у одного и того же субъекта для отслеживания динамики изменений, а также облегчает сбор образцов у педиатрических пациентов и других групп населения, для которых инвазивные процедуры могут быть нежелательны или невозможны. Это, в свою очередь, позволяет проводить эпидемиологические исследования и валидировать потенциальные биомаркеры СДВГ в больших когортах.
Исследования метаболомных профилей у пациентов с СДВГ выявили нарушения в ключевых метаболических путях, включая метаболизм катехоламинов, аминокислот и цикл мочевины. Нарушения в метаболизме катехоламинов, таких как дофамин и норадреналин, связаны с нарушениями нейротрансмиссии, часто наблюдаемыми при СДВГ. Изменения в метаболизме аминокислот, особенно незаменимых, могут указывать на нарушения в синтезе нейромедиаторов и других важных молекул. Нарушения в цикле мочевины, отвечающем за выведение азотистых отходов, свидетельствуют о потенциальных проблемах с общим метаболическим гомеостазом. Совместное нарушение этих путей предполагает, что СДВГ может быть связано с более широкой системной дисрегуляцией метаболизма, а не только с локальными изменениями в мозге.
Анализ сложных метаболомных данных требует применения продвинутых методов машинного обучения для выделения значимых биомаркеров. Это обусловлено высокой размерностью и сложностью метаболомных профилей, где количество измеряемых метаболитов значительно превышает количество исследуемых образцов. Алгоритмы машинного обучения, такие как метод главных компонент (PCA), метод опорных векторов (SVM), случайный лес (Random Forest) и нейронные сети, позволяют идентифицировать паттерны и корреляции, которые невозможно обнаружить с помощью традиционных статистических методов. Кроме того, для повышения точности и надежности результатов применяются методы перекрестной валидации и оптимизации параметров моделей.
Классификатор «Ближайшее сходство»: Новый подход к диагностике
Классификатор ближайшего соответствия (CR) представляет собой новый подход к обнаружению биомаркеров, объединяющий обучение интервальным признакам с мерой сходства на основе превосходства. Обучение интервальным признакам позволяет учитывать биологическую изменчивость, что повышает устойчивость идентификации биомаркеров. В основе метода лежит определение сходства между образцами не на основе точного равенства значений признаков, а на основе оценки превосходства одного образца над другим по каждому признаку, что позволяет более эффективно учитывать индивидуальные особенности и шум в данных. Это отличает CR-классификатор от традиционных методов машинного обучения, использующих, как правило, метрики расстояния или вероятностные модели.
Метод интервального обучения признакам учитывает естественную биологическую изменчивость, что повышает устойчивость идентификации биомаркеров. Вместо использования точных значений метаболитов, подход предполагает определение интервалов, в которых наблюдаются типичные значения для конкретной группы пациентов или контрольной группы. Это позволяет снизить влияние случайных колебаний и индивидуальных особенностей, которые могут искажать результаты анализа. Такой подход позволяет более надежно выявлять биомаркеры, поскольку он менее чувствителен к шуму и выбросам в данных, что особенно важно при анализе сложных биологических систем.
Для дальнейшей оптимизации набора биомаркеров в классификаторе CR используется отбор признаков, включающий жадный алгоритм отбора, управляемый методом Монте-Карло. Данный подход позволяет последовательно выбирать наиболее информативные метаболиты, оценивая их вклад в различимость между группами с использованием симуляций Монте-Карло для оценки статистической значимости. Жадный алгоритм отбора признаков итеративно добавляет метаболиты, максимизирующие различимость, до достижения оптимального набора, что обеспечивает повышение точности и снижение вычислительной сложности модели.
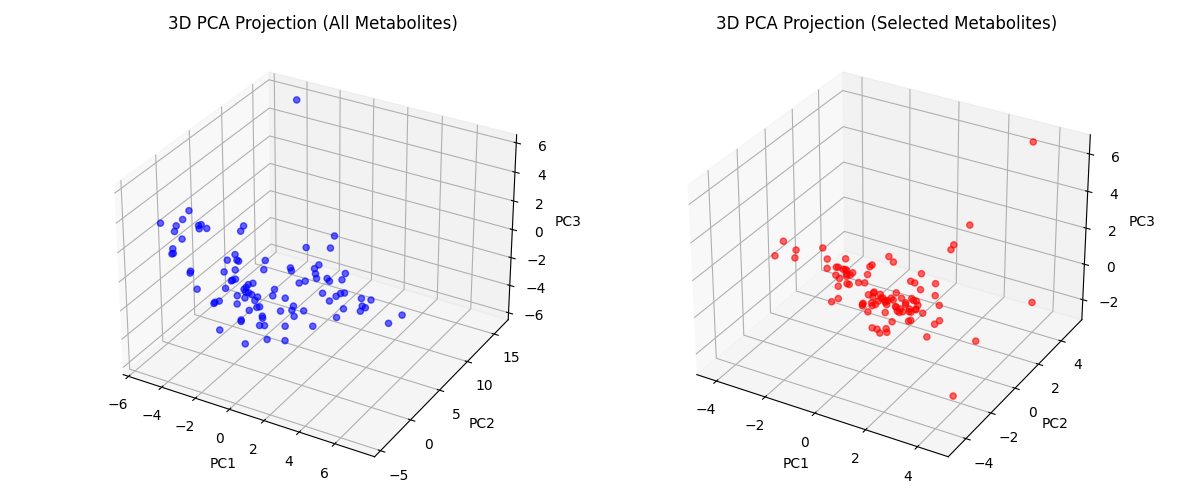
В ходе исследования, классификатор ближайшего соответствия (CR) продемонстрировал точность в 97,9% при дифференциальной диагностике пациентов с СДВГ и контрольной группы. Высокая точность была достигнута благодаря встроенному процессу отбора признаков, применённому к данным метаболомики мочи, и использованию всего 14 отобранных метаболитов. Данный результат превосходит показатели других протестированных моделей машинного обучения; в частности, классификатор Random Forest достиг точности в 91,8% при использовании всех 60 исследованных метаболитов.
При использовании всех 60 метаболитов классификатор CR достиг точности в 95.9%. Данный результат демонстрирует устойчивость и эффективность подхода, поскольку высокая точность классификации сохраняется даже при включении всего набора исходных данных, без необходимости предварительного отбора признаков. Это указывает на способность алгоритма эффективно использовать всю доступную информацию для дифференциации между группами, что важно для повышения надежности и обобщающей способности модели.
При использовании всех 60 метаболитов, классификатор Random Forest продемонстрировал точность в 91.8%. Данный результат получен в ходе сравнительного анализа с классификатором Closest Resemblance (CR), который, при тех же 60 метаболитах, достиг точности 95.9%. Несмотря на высокую точность, Random Forest уступает CR в эффективности идентификации пациентов с СДВГ в контрольной группе при использовании полного набора метаболитов.
К улучшению диагностики СДВГ и персонализированному лечению
Интеграция передовых методов машинного обучения, таких как классификатор CR, с метаболомным профилированием открывает перспективный путь к выявлению объективных и надежных биомаркеров для синдрома дефицита внимания и гиперактивности (СДВГ). Традиционная диагностика СДВГ часто основывается на субъективных оценках поведения, что может приводить к ошибкам и задержкам в начале лечения. Анализ метаболомного профиля, то есть состава метаболитов в биологических жидкостях, в сочетании с алгоритмами машинного обучения позволяет выявить специфические метаболические сдвиги, характерные для СДВГ. Это, в свою очередь, дает возможность разработать инструменты для более точной и ранней диагностики, а также для предсказания индивидуальной реакции на различные методы лечения, что является ключевым шагом к персонализированной терапии данного расстройства.
Разработка объективных биомаркеров для синдрома дефицита внимания и гиперактивности (СДВГ) открывает возможности для более ранней и точной диагностики, что имеет решающее значение для улучшения прогноза заболевания. Традиционные методы диагностики СДВГ часто опираются на субъективные оценки поведения, что может приводить к ошибкам и задержкам в постановке диагноза. Раннее выявление позволяет своевременно начать вмешательства, такие как поведенческая терапия или медикаментозное лечение, что, в свою очередь, способствует снижению негативного влияния СДВГ на учебную деятельность, социальную адаптацию и общее качество жизни пациента. Более точная диагностика также позволяет избежать ненужного назначения лекарств в тех случаях, когда симптомы могут быть связаны с другими состояниями, и, наоборот, обеспечить своевременное лечение тем, кто действительно нуждается в помощи.
Исследование метаболического профиля пациентов с синдромом дефицита внимания и гиперактивности (СДВГ) выявляет уникальные закономерности дисрегуляции метаболизма у каждого индивидуума. Вместо универсального подхода к лечению, становится возможным разработать персонализированные стратегии, учитывающие конкретные метаболические особенности пациента. Анализ метаболитов позволяет выявить ключевые биохимические пути, нарушенные у конкретного человека, что дает возможность подобрать наиболее эффективные терапевтические вмешательства — от диетотерапии и коррекции образа жизни до индивидуально подобранной фармакотерапии. Такой подход обещает не только повысить эффективность лечения, но и минимизировать побочные эффекты, значительно улучшая качество жизни пациентов с СДВГ.
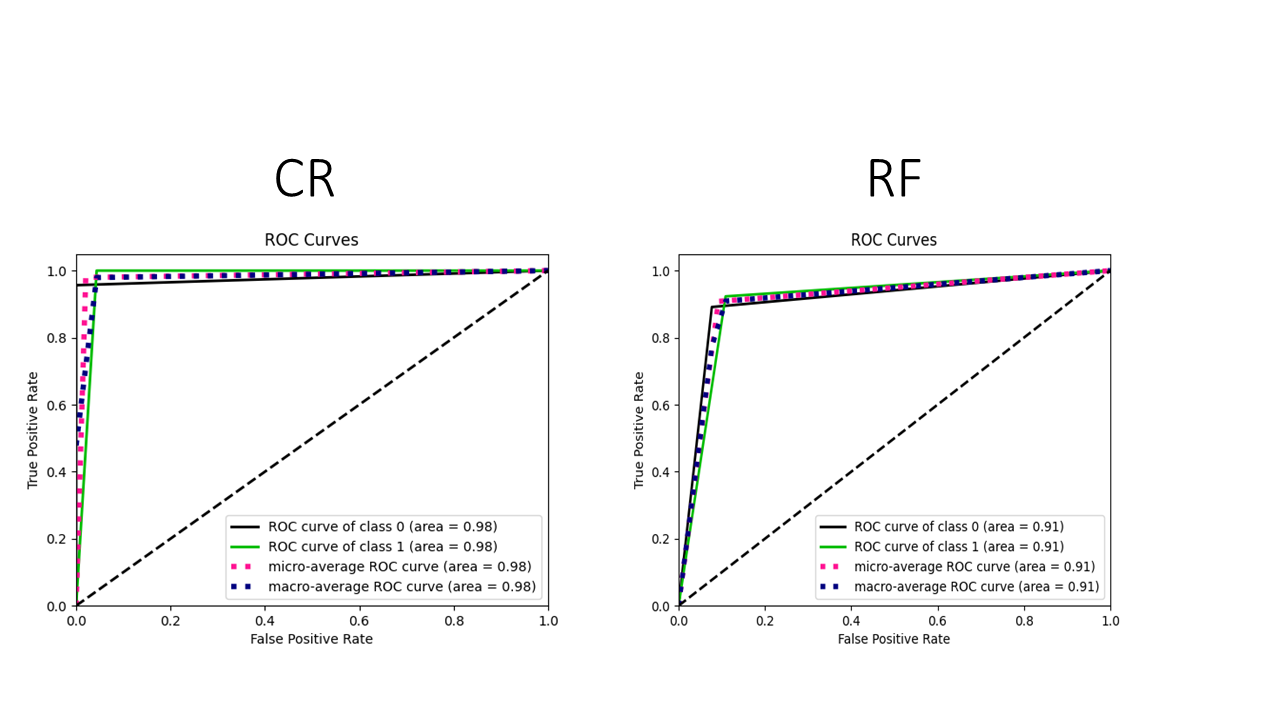
Разработанный классификатор CR продемонстрировал исключительно высокую способность к различению пациентов с синдромом дефицита внимания и гиперактивности (СДВГ) от контрольной группы. Оценка площади под ROC-кривой (AUC) составила 0.98 при использовании сокращенного набора метаболитов и 0.96 — при анализе всех 60 исследованных веществ. Эти результаты свидетельствуют о значительной диагностической точности и указывают на возможность использования метаболомного профилирования в качестве объективного инструмента для выявления СДВГ, что особенно важно для ранней диагностики и назначения эффективного лечения.
Для успешного внедрения полученных результатов в клиническую практику и улучшения качества жизни людей с синдромом дефицита внимания и гиперактивности, необходимы дальнейшие углубленные исследования и валидация выявленных метаболических биомаркеров. Особое внимание следует уделить проспективным исследованиям с участием больших когорт пациентов, а также изучению долгосрочной стабильности и надежности этих маркеров в различных популяциях. Важным этапом станет разработка стандартизированных протоколов для сбора и анализа метаболомных данных, что обеспечит воспроизводимость результатов в различных лабораториях. Только комплексный подход, включающий как фундаментальные исследования, так и клинические испытания, позволит в полной мере реализовать потенциал объективных биомаркеров для ранней диагностики и персонализированного лечения СДВГ.
Исследование, посвящённое выявлению метаболических биомаркеров СДВГ, закономерно напоминает попытку приручить хаос. Авторы используют алгоритм CR с встроенным отбором признаков, стремясь к интерпретируемости — благородная цель, учитывая, что в конечном итоге, система всегда найдёт способ сломать элегантную теорию. Этот подход к выявлению биомаркеров в моче, хоть и кажется сложным, лишь подтверждает старую истину: даже самые передовые методы — это лишь инструменты. Как метко заметил Брайан Керниган: «Простота — это главное. Сложность — это признак плохого дизайна». И пусть эта простота не всегда достижима, стремление к ней — залог хоть какой-то стабильности в мире постоянно меняющихся технологий и алгоритмов.
Что дальше?
Представленный подход к поиску метаболических биомаркеров СДВГ, безусловно, элегантен. Однако, стоит помнить, что «интерпретируемость» в машинном обучении — понятие зыбкое. Красивые диаграммы, демонстрирующие вклад отдельных метаболитов, неизбежно усложнятся, когда данные выйдут за рамки контролируемого эксперимента. Продакшен всегда найдёт способ превратить лаконичный классификатор в монолит, который никто не сможет отладить.
Более того, сама идея поиска единого набора «диагностических» метаболитов выглядит несколько наивно. СДВГ — гетерогенное расстройство, и, вероятно, у каждого пациента будет свой уникальный метаболический профиль. Вместо того чтобы стремиться к универсальному решению, стоит сосредоточиться на разработке персонализированных моделей, учитывающих индивидуальные особенности каждого пациента. Если тесты зелёные — значит, они ничего не проверяют, а лишь подтверждают, что входные данные соответствуют ожидаемым.
В конечном итоге, успех этой работы будет зависеть не столько от точности классификатора, сколько от способности интегрировать метаболомные данные с другими источниками информации — генетическими, поведенческими, клиническими. И, разумеется, от готовности признать, что любая «революционная» технология завтра станет техдолгом. Всё это уже было в 2012-м, только называлось иначе.
Оригинал статьи: https://arxiv.org/pdf/2601.11283.pdf
Связаться с автором: https://www.linkedin.com/in/avetisyan/
Смотрите также:
- Квантовый Борьба: Китай и США на Передовой
- Укрощение шума: как оптимизировать квантовые алгоритмы
- Интеллектуальная маршрутизация в коллаборации языковых моделей
- Квантовая химия: моделирование сложных молекул на пороге реальности
- Квантовые симуляторы: проверка на прочность
- Квантовые нейросети на службе нефтегазовых месторождений
- Искусственный интеллект заимствует мудрость у природы: новые горизонты эффективности
2026-01-19 19:10